용액의 농도
-
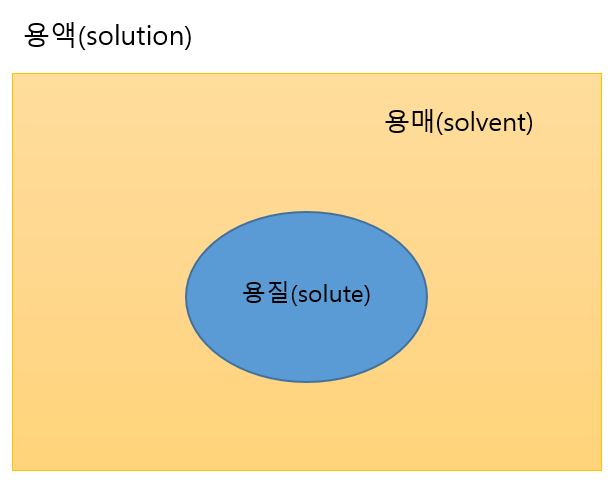
용액(solution)
두가지 이상의 물질이 섞어서 균일한 상태를 이룬 것. 용매∪용질 = 용액
- 용매(solvent) : 용매 = 용액 - 용질
- 용질(solute) : 용질 = 용액 - 용매
※ - : 차집합
※ 분자 간 상호작용이 크면 잘 녹거나 잘 섞이고, 반대로 작으면 잘 녹지도 섞이지도 않는다. ex) 극석이 높은 물은 Na+,Cl− 등 이온을 잘 둘러싸서 안전화 시킨다.(물에 소금이 잘 녹는다.)
퍼센트 농도 => 질량비
(%)=mass of solutionmass of solute×100
용액보다 용질이 매우 적을 시에는 ppm(parts per million)이나 ppb(parts per billion) 을 사용한다.
ppm=mass of solutionmass of solute×106
ppb=mass of solutionmass of solute×109
몰 분율(mole fraction)
용매의 몰 분율(X1) = # of moles of solvent + # of moles of solute# of mole of solvent
용질의 몰 분율(X2) = # of moles of solvent + # of moles of solute# of mole of solute
X1+X2=1
몰 농도(Molarity)
몰 농도(M) = volumeofsolution# of mole of solute
※ 몰 농도는 M 으로 표기하고 몰랄 농도는 m으로 소문자와 대문자로 표기하기에 강조하기 위해 빨간색으로 표기하였다.
※ 몰 농도를 이용하면 용액속에 녹아있는 용질의 양(mol) 과 질량을 구할 수 있다.
ex) 0.1M 수산화 나트륨 NaOH 수용액 100ml 를 만들기 위한 수산화 나트륨의 질량
0.1L×0.1mol/L=0.01mol
0.01mol×40g/mol=0.4g
몰랄 농도(molarity)
※몰 농도는 부피를 기준으로하기 때문에 온도에 따라 변화함. 온도 변화에 관계 없이 일정한 농도가 필요할 시 몰랄 농도 사용
몰랄 농도(m) =kg of solventmol of solute


