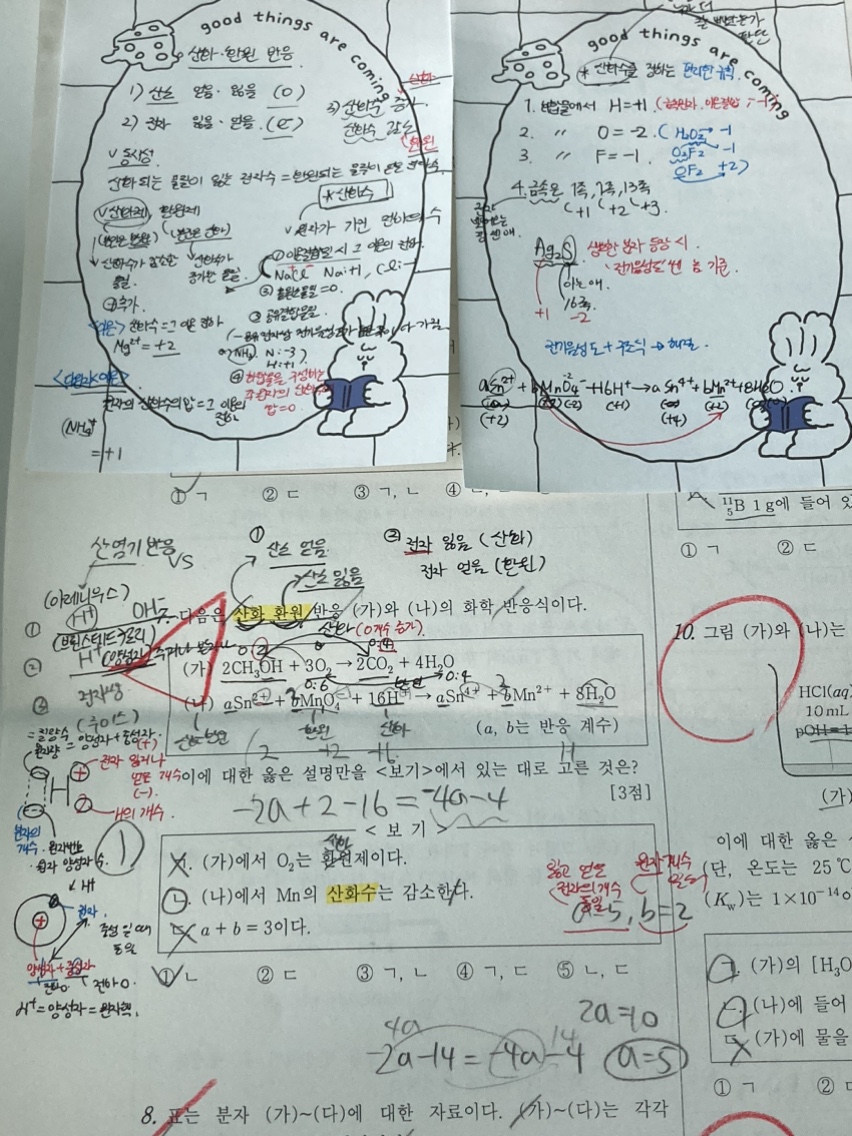
1.문제 분석
-산화 환원 반응
🥹산화 환원이 어떤 반응인지 모른 게 가장 큰 문제
Sol. 왜 잘 몰랐을까?
산염기 반응에서 양성자( H+) 와 헷갈림.
그럼 의미로 산 염기 반응과 산화 환원 반응을 정리하고 가자.
산 염기는 양성자와 전자쌍이 관여하는 반응
산화환원은 전자가 관여
산화환원 동시성은 아는 내용이니 넘어가고
산화제 환원제는 본인이 산화되면 환원제
본인이 환원되면 산화제
산화수란?
원자가 가진 전하 수.
당연히 홑원소물질=0.
이온에서는 산화수가 그 이온 전화
다원자이온에서는 원자의 산화수의 합= 그 이온의 전하.
공유결합 물질에서는 전기음성도가 큰 물질이 공유전자쌍을 다 뺏어옴
!화합물을 구성하는 각 원자의 산화수의 합=0.
🪐산화수를 정하는 편리한 규칙🪐
1.화합물에서 H=+1 ((공유결합에서, 대체적으로 원자를 잘 뺏기니까))
2. 화합물에서 O= -2
아 근데 예외 있음,
H2o2,,,-1
O2F2,,-1
OF2,,+2
3. 화합물에서 F=-1
4.금속은 1족 2족 13족
+1,+2,+3
생소하고 모르는 새끼 등장 시
전기 음성도+구조식 쓰면 끝
원소 표기법.
H+ 같은 경우 전자를 잃은/얻은 개수를 나타냄.