Determination of and
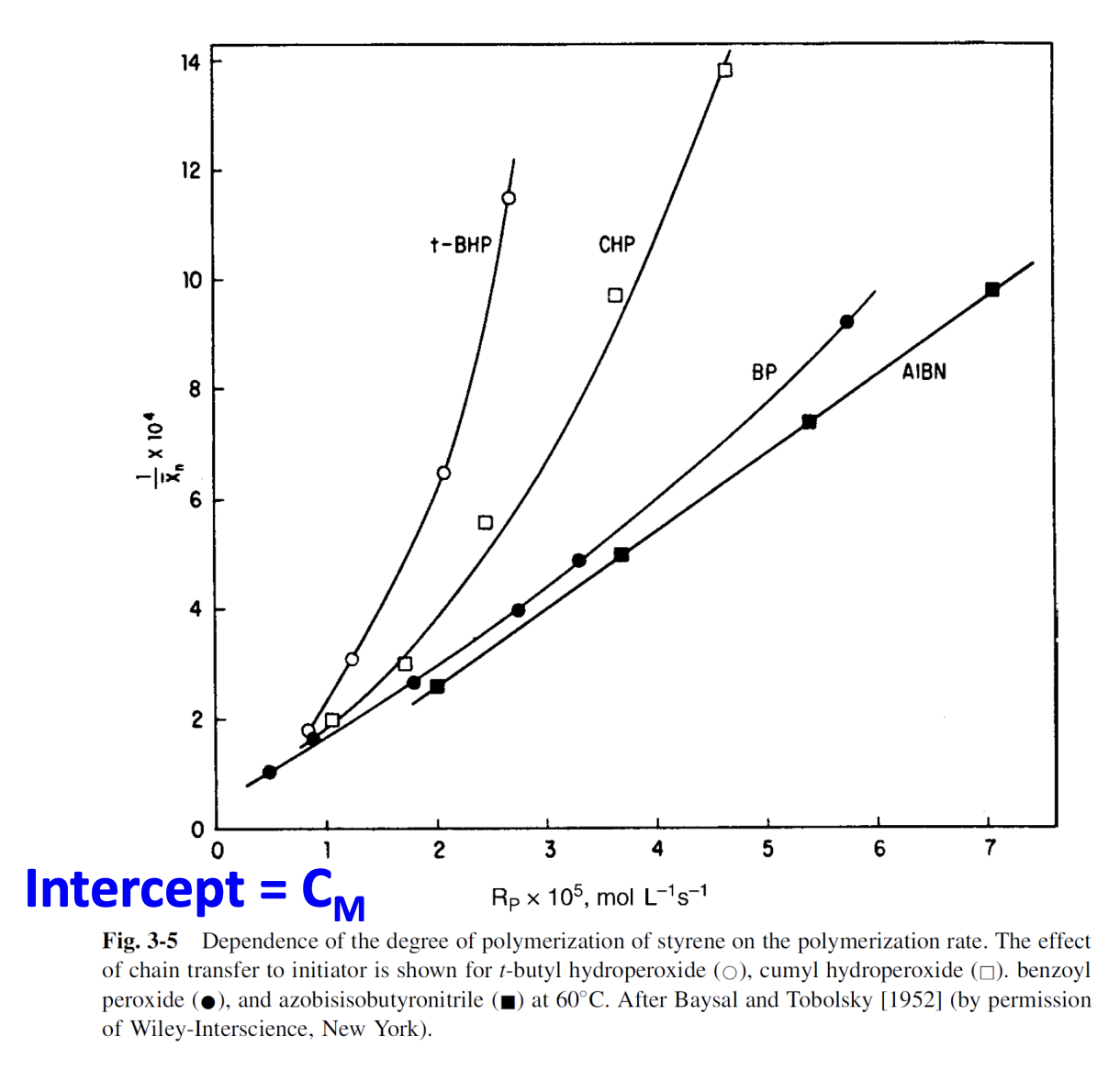
위 그래프는 축을 로 두고 축을 으로 둔 뒤 plot한 그래프이다. 개시제의 종류에 따라 선형적인 관계를 따르기도 하고 비선형 관계를 따르는 것으로 나타난다. 그 이유는 무엇일까? 개시제의 종류에 따라 chain transfer가 개시제로 더 많이 일어나는 경우에는 term의 의 영향을 더 받게 되고, 비교적 monomer로 chain transfer가 일어나는 경우에는 의 영향을 더 많이 받기 때문이다. 위 그래프에서는 t-BHP와 CHP는 BP와 AIBN보다 chain transfer가 더 많이 일어나기 때문에 개시제로 chain transfer가 일어남에 따라 고분자의 molecular weight가 같은 중합 속도에서도 더 낮음을 확인할 수 있다. 그리고 위와 같은 그래프에서 절편이 에 해당하는 값임을 알 수 있다.
만약 monomer로 chain transfer가 일어나는 것과 chain transfer agent에 의한 chain transfer를 무시할 수 있다면, Mayo equation은 아래와 같이 다시 표현될 수 있다.
위 식에서 을 로 좌변을 로 선형회귀/외삽으로 plot하게 되면 아래와 같은 그래프가 되고, 이때 기울기가 임을 알 수 있다.
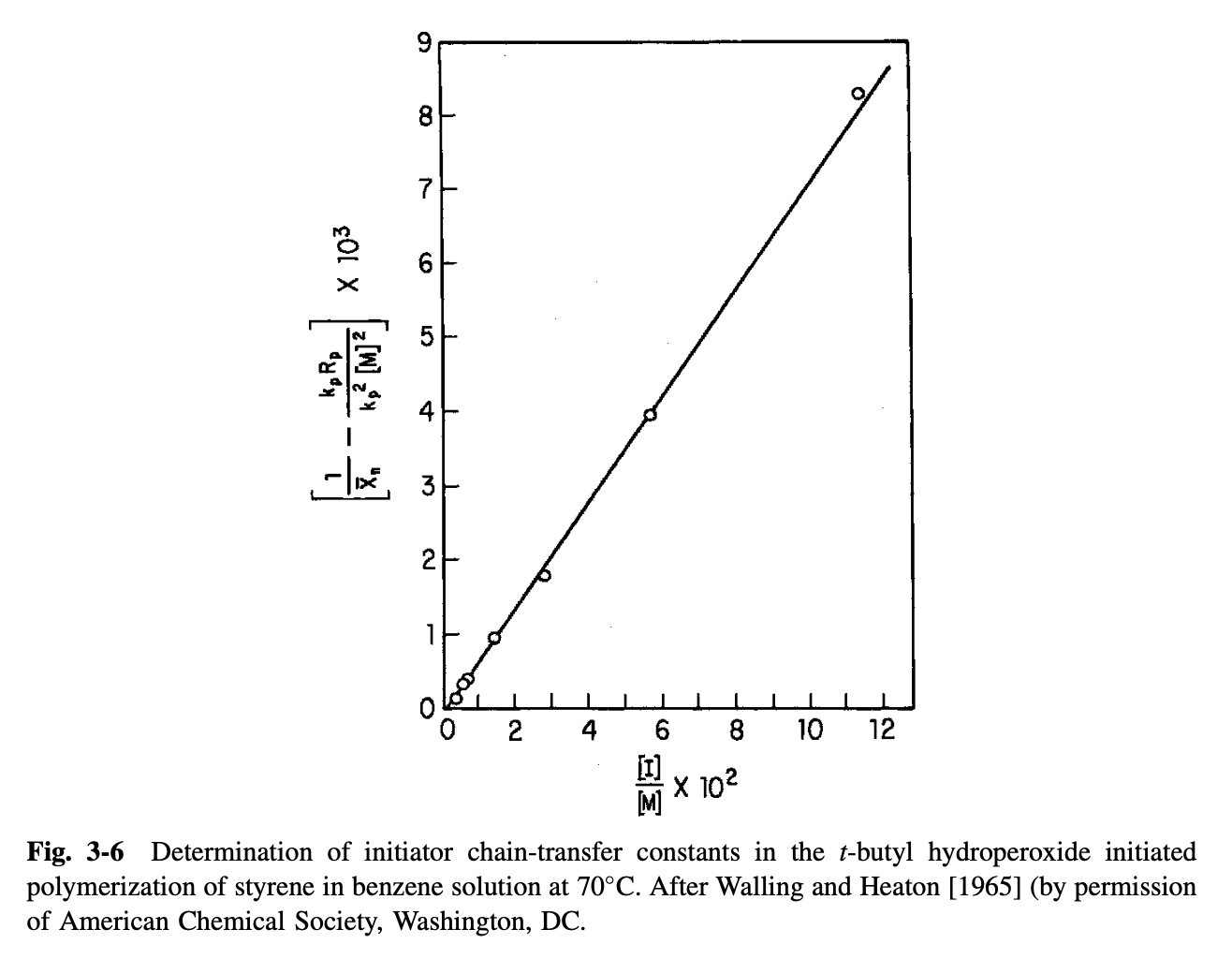
Monomer Transfer Constants
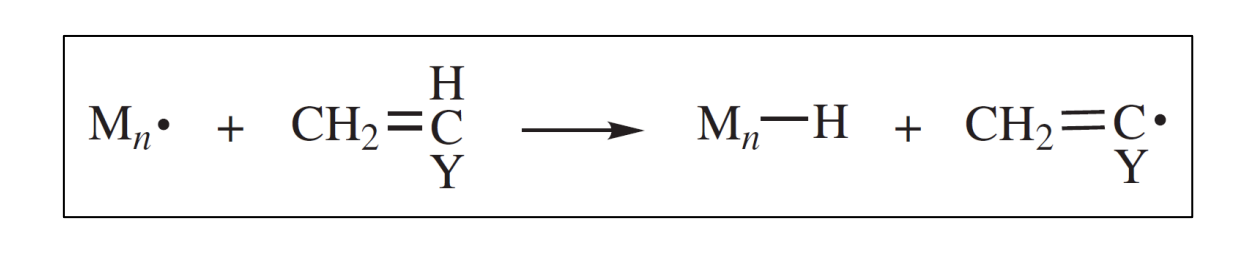
monomer로 chain transfer가 일어나는 경우를 반영하는 상수 값인 은 대부분의 monomer에 대해 아주 작은 값을 갖는다. 대부분이 정도의 값을 갖는데, 그 이유는 monomer로 chain transfer가 될 때, 강한 vinyl 탄소-수소 결합이 깨지는 것을 포함하기 때문이다. 탄소-수소 간의 강한 이중 결합을 깨뜨리는데 많은 에너지를 필요로 하기에 일어나기 쉬운 반응이 아니다. 그렇기에 은 아주 작은 값을 갖게 된다. 아래의 도식도가 chain transfer to monomer의 반응을 보여준다.
하지만 예외로 큰 의 값을 갖는 경우도 존재하는데, 그 이유는 propagating radical의 반응성이 상당히 높은 경우이다. 아래와 같이 vinyl acetate의 chain transfer 반응을 보면 vinyl acetate로부터 생성된 라디칼의 반응성이 매우 높기에 의 값이 커져 가 큰 값을 가질 수 있게 된다.
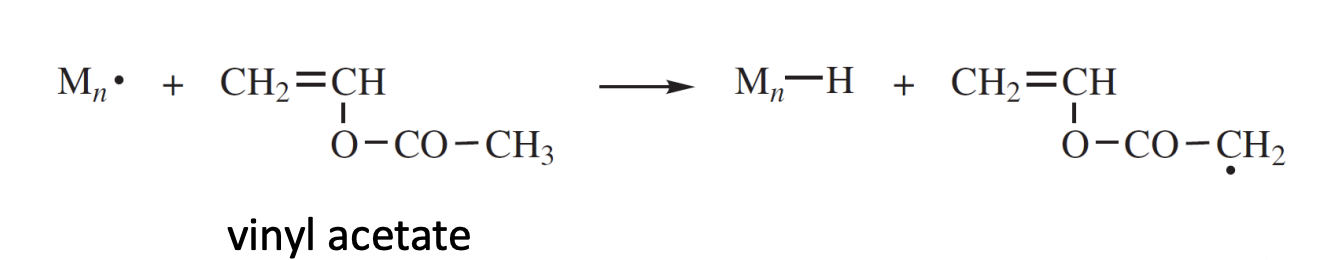
Initiator Transfer Constants
Mayo equation에서 chain transfer agent가 존재하지 않는다고 가정하면, 이 된다. 그럼 Mayo equation은 아래와 같이 쓸 수 있다.
이때 라디칼 체인 중합에서 monomer로 styrene을 사용하고, initiator로 Benzoyl Peroxide(BPO)를 사용한 경우를 가정해보자. 위 중합 과정에서 측정 결과로 로 얻어진다. 즉, 값에 비해 값이 매우 작기에 무시할 만하다. 그리고 에 의한 영향으로 수평균 중합도는 더욱 감소하기 때문에, 고분자의 molecular weight를 높이기 위해 가 보다 작은 다른 개시제를 사용하는 방법을 고안할 수 있다. 하지만 이 결론이 맞다고 볼 수 없는 이유는 값의 변화가 수평균 중합도에 영향을 크게 주지 못한다. 개시제의 농도 이므로 가 낮아져도, 에는 큰 영향을 주지 못할 것이다.
아래의 표는 의 값을 어떤 monomer를 중합하는 지와 어떤 initiator를 사용하는 지에 따라 표기한 것이다.
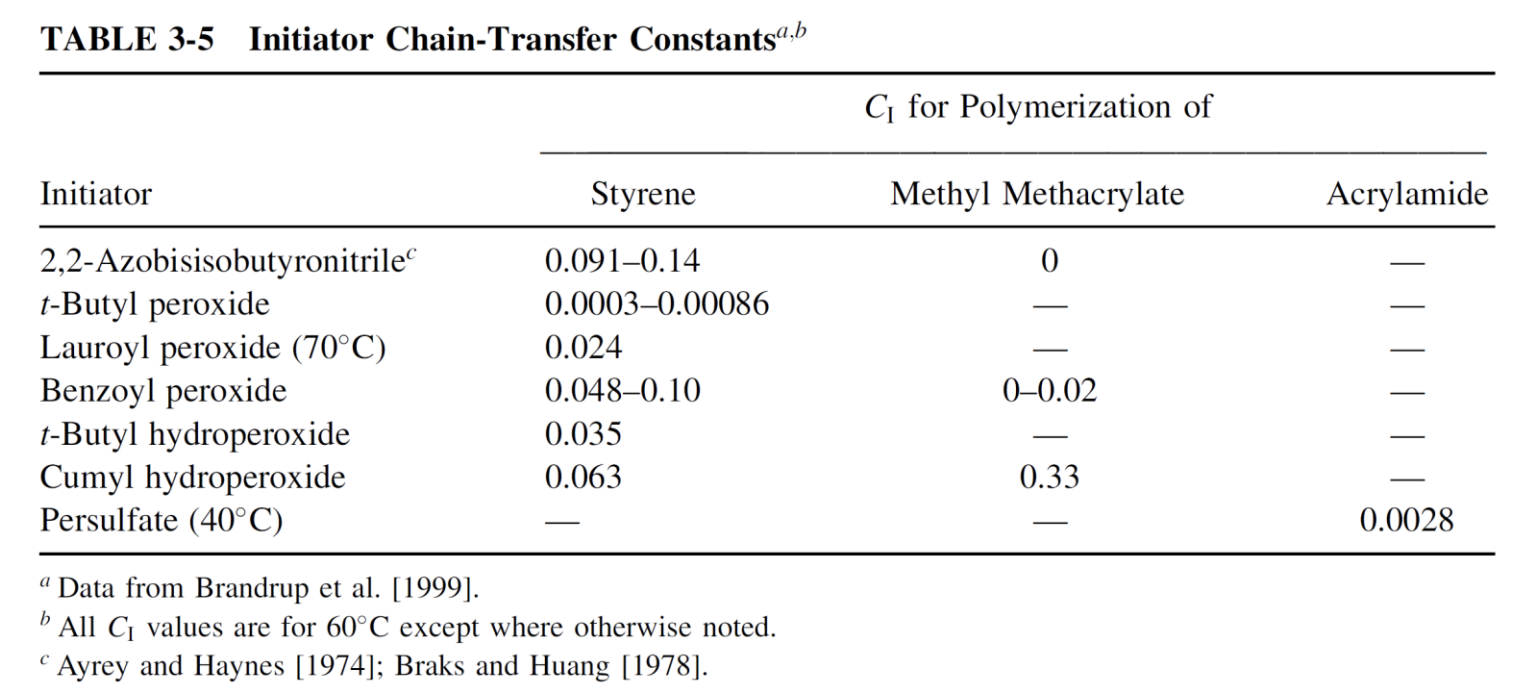
가 어떤 개시제를 사용하냐에 따라 달라지는 이유는 propagating radical의 반응성의 차이로 인해 달라진다. 또한 는 같은 개시제를 사용하여도 어떤 monomer를 중합하냐에 따라 달라질 수 있다.
